Presentacin de PowerPoint PowerPoint PPT Presentation
1 / 18
Title: Presentacin de PowerPoint
1
(No Transcript)
2
TRIÁNGULO DEL ENLACE
IÓNICO
METÁLICO
COVALENTE
3
(No Transcript)
4
(No Transcript)
5
- Momento dipolar
- Deducción de estructuras moleculares
- Causado por una distribución de densidad
electrónica no uniforme en la molécula.
?0
?gt0
En el enlace
? ? dAB
A B
Cm ó D (debye)
?
?-
donde ?Alt ?B
El momento dipolar de enlace es un vector!!
6
?C-Hgt0 momento dipolar de enlace pero ?T0
Una molécula es polar si el momento dipolar total
es diferente de 0. Lo anterior ocurre, si y solo
si, la suma vectorial de los momentos dipolares
de enlace es diferente a 0
CHCl3 ?T 1.01 Polar
CH2Cl2 ?T 1.6 Polar
CH3Cl ?T 1.87 Polar
CCl4 ?T0 No polar
7
Agua ?T1.85 Polar
Éter metílico ?T1.15 Polar
MeOH ?T1.7 Polar
Acetona ?T2.88 Polar
Dimetilsulfóxido ?T3.93 Polar
hexano ?T0.012
?
Ciclohexano ?T0 No Polar
Silla Bote
8
Ejercicios -Ordenar a las anteriores moléculas
de la menos polar a las más polar -Para las
siguientes moléculas indicar cual de ellas es
polar (contiene dipolo permanente) H2S NH3
BeH2 SF6 etèr etìlico tolueno etanol
disulfuro de carbono I2
9
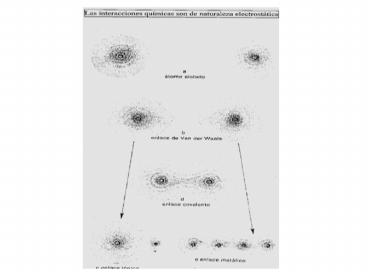
INTERACCIONES QUÍMICAS
INTERACCIÓN ION-ION Interacción
omnidireccional, muy fuerte y opera a larga
distancia INTERACCIÓN COVALENTE Interacc
ión es direccional, muy fuerte y opera a cortas
distancias Traslape
10
INTERACCIÓN ION-DIPOLO Interacción
direccional, fuerte y opera a distancias
cortas. INTERACCIÓN DIPOLO-DIPOLO Inte
racción direccional, de fuerza moderada y opera a
distancias cortas
11
INTERACCIÓN ION-DIPOLO INDUCIDO Inter
acción direccional, débil y opera a distancias
muy cortas
- Polarización (reglas de Fajans)
- Catión. Carga alta y tamaño pequeño mas
polarizante
P.I. Z/r (potencial iónico) - Anión. Carga alta y tamaño pequeño mas
polarizable
12
INTERACCIÓN DIPOLO-DIPOLO INDUCIDO I
nteracción direccional, muy débil y opera a
distancias extremadamente cortas
13
INTERACCIÓN DIPOLO INSTANTÁNEO-DIPOLO
INDUCIDO Interacción direccional,
muy débil y opera a distancias muy cortas.
14
INTERACCIONES POR PUENTE DE HIDRÓGENO Cuando
el átomo de hidrógeno está enlazado a dos
átomos Átomos muy electronegativos
Generalmente, se presenta un enlace corto
(covalente ) y un enlace largo y más
débil H-F-------F O-H-------O O-H-------F
O-H-------N N-H-------Cl N-H-------S
15
FUERZAS DE REPULSIÓN Solo son
importantes a distancias extremadamente
cortas
16
(No Transcript)
17
(No Transcript)
18
(No Transcript)