Nessun titolo diapositiva - PowerPoint PPT Presentation
1 / 30
Title:
Nessun titolo diapositiva
Description:
Vibrazioni permesse per una molecola n-atomica vibrazioni = 3 n - (rotazioni + traslazioni) Rotazioni e traslazioni sono sempre 3 ad eccezione di una molecola ... – PowerPoint PPT presentation
Number of Views:35
Avg rating:3.0/5.0
Title: Nessun titolo diapositiva
1
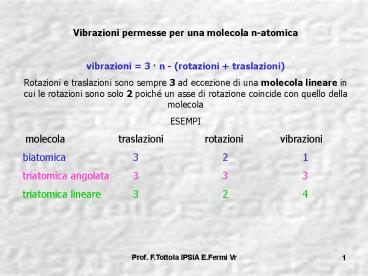
Vibrazioni permesse per una molecola
n-atomica vibrazioni 3 n - (rotazioni
traslazioni) Rotazioni e traslazioni sono sempre
3 ad eccezione di una molecola lineare in cui le
rotazioni sono solo 2 poiché un asse di rotazione
coincide con quello della molecola ESEMPI
molecola traslazioni
rotazioni vibrazioni biatomica 3
2 1 triatomica angolata 3
3 3 triatomica lineare 3
2 4
2
- Le vibrazioni teoriche non danno luogo ad
altrettanti assorbimenti poiché - possono avvenire senza variazione del momento di
dipolo - lassorbimento può cadere al di fuori del campo
studiato - più vibrazioni possono causare un unico
assorbimento - alcune vibrazioni danno assorbimenti così vicini
da non essere risolvibili - alcune vibrazioni teoriche sono solo apparenti
3
- Gli assorbimenti reali possono anche essere
maggiori di quelli teoricamente prevedibili
perché possono verificarsi - degli overtones, cioè assorbimenti a frequenze
multiple di un dato assorbimento poiché la loro
intensità cala rapidamente con laumentare
dellordine sono osservabili solo alcuni di
quelli con frequenza doppia - delle bande di combinazione, dovute a transizioni
su livelli vibrazionali la cui energia è uguale
alla combinazione delle energie di due livelli
diversi - accoppiamenti rotovibrazionali, tipici di
spettri di gas e vapori, che danno luogo a bande
tripartite
4
MOLECOLA TRIATOMICA LINEARE CON DUE ATOMI
UGUALI CO2
5
attivo perché si ha variazione del momento di
dipolo
6
Inattivo perché non si ha variazione del momento
di dipolo
7
Le due vibrazioni coincidono (in realtà la
molecola è sempre nel piano) e quindi danno un
unico assorbimento
8
Entrambe degenerano in rotazioni e non sono da
considerare
9
Pertanto le quattro vibrazioni teoriche di CO2
sono
- Stretching asimmetrico (na)
- Stretching simmetrico (ns)
- Wagging (w)
- Scissoring (d)
INATTIVO
COINCIDONO
delle quali pertanto se ne osservano solo due
10
MOLECOLA TRIATOMICA LINEARE CON TUTTI ATOMI
DIVERSI HCN
11
attivo perché varia la distanza tra le cariche e
quindi il momento di dipolo
12
attivo perché varia la distanza tra le cariche e
quindi il momento di dipolo
13
Le due vibrazioni coincidono (in realtà la
molecola è sempre nel piano) e quindi danno un
unico assorbimento
14
Entrambe degenerano in rotazioni e non sono da
considerare
15
Pertanto le quattro vibrazioni teoriche di HCN
sono
- Stretching asimmetrico (na)
- Stretching simmetrico (ns)
- Wagging (w)
- Scissoring (d)
COINCIDONO
delle quali pertanto se ne osservano solo tre.
16
MOLECOLA TRIATOMICA NON LINEARE CON DUE ATOMI
UGUALI H2O
17
attivo perché varia la distanza tra le cariche e
quindi il momento di dipolo
18
attivo perché varia la distanza tra le cariche e
quindi il momento di dipolo
19
attivo perché varia la distanza tra le cariche e
quindi il momento di dipolo
20
Tutte degenerano in rotazioni e non sono da
considerare
21
Pertanto le tre vibrazioni teoriche di H2O sono
- Stretching asimmetrico (na)
- Stretching simmetrico (ns)
- Scissoring (d)
che si osservano tutte.
22
- Se si fa riferimento a una porzione di una
molecola con più atomi, la sua complessità fa sì
che si possano riscontrare effettivamente tutte
le vibrazioni teoriche. - deformazioni (bending)
- che possono avvenire
- nel piano
- fuori del piano
- stiramenti (stretching )
- Entrambi i tipi di vibrazione possono esssere
- simmentrici
- asimmetrici
23
(No Transcript)
24
(No Transcript)
25
(No Transcript)
26
(No Transcript)
27
(No Transcript)
28
(No Transcript)
29
(No Transcript)
30
(No Transcript)