Das ideale Gas PowerPoint PPT Presentation
Title: Das ideale Gas
1
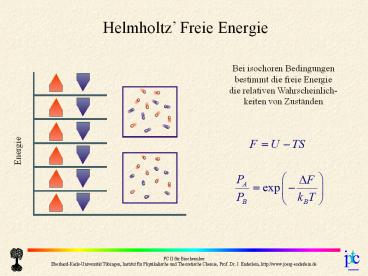
Bei isochoren Bedingungen bestimmt die freie
Energie die relativen Wahrscheinlich- keiten von
Zuständen
Energie
2
Bei isobaren Bedingungen bestimmt das
GibbsscheThermodynamische Potential die
relativen Wahrscheinlich- keiten von Zuständen
Enthalpie
3
Innere Energie U
Enthalpie H
Helmholtz Freie Energie F
Gibbs Thermodyn. Pot. G
4
Helmholtz Freie Energie F
Gibbs Thermodyn. Pot. G
Isochore Bedingungen
Isobare Bedingungen
5
Schnelle Expansion eines Gases
p1, T1
p2, T2
Für ideales Gas
T1 T2 !
Für reales Gas?
6
p1, T1, V1
p2, T2, V2
Uns interessierende Größe
?
H
Energiebilanz
7
Wir wählen p und T als die unabhängigen
Zustandsgrößen
8
(No Transcript)
9
Suche thermodynamische Funktion U, F, H, G, deren
Differential S vor und p nach dem
Differentialoperator hat
10
(No Transcript)
11
Ideales Gas
12
Van-der-Waals-Gas
13
Van-der-Waals-Gas
14
Van-der-Waals-Gas
wenn
wenn
und
Inversionstemperatur
15
(No Transcript)
16
An welcher Stelle findet Phasenübergang statt?
Molares Gibbssches Thermodynamisches Potential
Chemisches Potential
17
An welcher Stelle findet Phasenübergang statt?
Phasengleichgewicht
18
Maxwell-Konstruktion
19
Vg
Vl
Latente Wärme L
Entropieänderung
PowerShow.com is a leading presentation sharing website. It has millions of presentations already uploaded and available with 1,000s more being uploaded by its users every day. Whatever your area of interest, here you’ll be able to find and view presentations you’ll love and possibly download. And, best of all, it is completely free and easy to use.
You might even have a presentation you’d like to share with others. If so, just upload it to PowerShow.com. We’ll convert it to an HTML5 slideshow that includes all the media types you’ve already added: audio, video, music, pictures, animations and transition effects. Then you can share it with your target audience as well as PowerShow.com’s millions of monthly visitors. And, again, it’s all free.
About the Developers
PowerShow.com is brought to you by CrystalGraphics, the award-winning developer and market-leading publisher of rich-media enhancement products for presentations. Our product offerings include millions of PowerPoint templates, diagrams, animated 3D characters and more.