ELECTROCHEMISTRY - PowerPoint PPT Presentation
1 / 56
Title: ELECTROCHEMISTRY
1
?????????
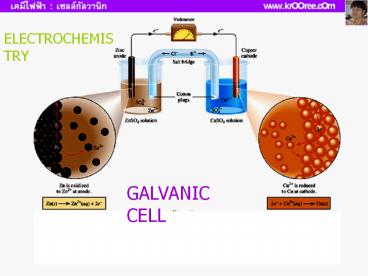
ELECTROCHEMISTRY
?????????????
GALVANIC CELL
???????????? ????????????????
?????????????????????????? ????????
2
????????????? ??????????????????????????? ????????
???????????????????????????? ?????????????????????
??????????????????????????????? ????????????????
(Nernst Equation) ?????????????????????????
-
?????????? - 1. ???????????????????????????????????????????
?????????????????????????? - ??????????????????????????????????????????????????
???????????????????????????? - ??????????????????????????????????????????????????
????????????????????????????????? - ???????????????????????????????????????????? (E?)
????????? E? ???????????? - ????????????????????????????????????????????
?????? - 5. ??????????????????????????????
3
Electron Transfer Reactions
- Electron transfer reactions are
oxidation-reduction or redox reactions. - Results in the generation of an electric current
(electricity) or be caused by imposing an
electric current. - Therefore, this field of chemistry is often
called ELECTROCHEMISTRY.
4
Why Study Electrochemistry?
- Batteries
- Corrosion
- Industrial production of chemicals such as
Cl2, NaOH, F2 and Al - Biological redox reactions
5
Electrochemical Cells
chemical change electric current
electric current chemical change
GALVANIC CELL
ELECTROLYTIC CELL
VOLTAIC CELL
6
??????? ???????????????????????????????
???? ?????????? 1. ??????????????????????
???????????????????????????????????? 2.
????????????????????????????????
3. ??????????????????????????????????
??? 4. ??????????????????????????????????????
?????????????? 5. ?????????????????????????????
?
7
??????????
Zn(s)/Zn2(aq)
Cu(s)/Cu2(aq)
?????????
1. ???????????? Zn(s)/Zn2(aq) ???
Cu(s)/Cu2(aq) ???????????
?????????????(????????????????? KNO3?????????????
??????????????????????????????????????????????????
????
2. ??????????????????????????????????????????????
?????????????????????????????????????
???????????????????
3. ??????????????????????? ???????????????????????
??????????????
???????????????????
4. ????????? 1.0 V ???????????????
???????????????????
8
Galvanic cell
2
krooree _at_ pcccr.ac.th
??????????
Zn(s)/Zn2(aq)
Cu(s)/Cu2(aq)
?????????
5. ?????????????????????? 1-4
????????????????????????????????????
????????????????????????????????
??????????
Mg(s)/Mg2(aq)
Cu(s)/Cu2(aq)
Mg(s)/Mg2(aq)
Zn(s)/Zn2(aq)
Fe(s)/Fe2(aq)
Cu(s)/Cu2(aq)
Fe(s)/Fe2(aq)
Zn(s)/Zn2(aq)
Fe(s)/Fe2(aq)
Mg(s)/Mg2(aq)
9
e-
e-
Anode
Cathode
Cu2 (aq) 2e- ? Cu(s)
Zn(s) ? Zn2(aq) 2 e-
Zn(s) Cu2(aq) ? Zn2(aq) Cu(s)
10
???????????????????????????
1. ????????????????????????? ??????????????????(
) ?????????????????????????
11
???????????????????????????
2. ?????????????????
-?????????????????????????????????????????????????
?
-???????????????????????????????????????????????
-?????????????????????????? ???? (s) (aq) (l)
-???????????????????? ??????????? ??????????(/)
-????????????????????? ??????????? ??????(,)
Pt(s) / Fe3(aq) , Fe2(aq)
3. ???????????????????????
-?????????????????????????????????????????????????
?????????????????????
Pt(s)/H2(g, 1 atm)/H(aq)
4. ???????????????????????????????????????????????
? ????
Mg(s)/Mg2(aq, 1 mol/dm3 )//Fe3(aq, 1
mol/dm3),Fe2(aq,1mol/dm3)/Pt(s)
12
e-
e-
cathode
anode
half cell
Cu(s)/Cu2(aq)
Zn(s)/Zn2(aq)
half reaction
Cu2(aq) 2e- ? Cu(s)
Zn(s) ? Zn2(aq) 2e-
redox reaction
Zn(s) Cu2(aq) ? Zn2(aq) Cu(s)
cell notation
Zn(s) / Zn2(aq) // Cu2(aq) / Cu(s)
13
e-
e-
cathode
anode
half cell
Cu(s)/Cu2(aq)
Mg(s)/Mg2(aq)
half reaction
Cu2(aq) 2e- ? Cu(s)
Mg(s) ? Mg2(aq) 2e-
redox reaction
Mg(s) Cu2(aq) ? Mg2(aq) Cu(s)
cell notation
Mg(s) / Mg2(aq) // Cu2(aq) / Cu(s)
14
e-
e-
cathode
anode
half cell
Zn(s)/Zn2(aq)
Mg(s)/Mg2(aq)
half reaction
Zn2(aq) 2e- ? Zn(s)
Mg(s) ? Mg2(aq) 2e-
redox reaction
Mg(s) Zn2(aq) ? Mg2(aq) Zn(s)
cell notation
Mg(s) / Mg2(aq) // Zn2(aq) / Zn(s)
15
e-
e-
anode
cathode
half cell
Fe(s)/Fe2(aq)
Cu(s)/Cu2(aq)
half reaction
Fe(s) ? Fe2(aq) 2e-
Cu2(aq) 2e- ? Cu(s)
redox reaction
Fe(s) Cu2(aq) ? Fe 2(aq) Cu(s)
cell notation
Fe(s) / Fe2(aq) // Cu2(aq) / Cu(s)
16
e-
e-
cathode
anode
half cell
Fe(s)/Fe2(aq)
Zn(s)/Zn2(aq)
half reaction
Fe2(aq) 2e- ? Fe(s)
Zn(s) ? Zn2(aq) 2e-
redox reaction
Zn(s) Fe2(aq) ? Zn2(aq) Fe(s)
cell notation
Zn(s) / Zn2(aq) // Fe2(aq) / Fe(s)
17
e-
e-
anode
cathode
half cell
Mg(s)/Mg2(aq)
Fe(s)/Fe2(aq)
half reaction
Mg(s) ? Mg2(aq) 2e-
Fe2(aq) 2e- ? Fe(s)
redox reaction
Mg(s) Fe2(aq) ? Mg2(aq) Fe(s)
cell notation
Mg(s) / Mg2(aq) // Fe2(aq) / Fe(s)
18
???????????????????
?????????????? 9.3 ????????
19
???????????? 9.3 ??? 1 (?)
?????????????????????????????????
????????????????????????????????????? ?????????
?????????????????????????
Sn(s)Sn2 (aq) Cu2(aq)Cu(s)
????????????
Sn(s) ? Sn2 (aq) 2e-
????????????
Cu2(aq) 2e- ? Cu(s)
?????????????????
Sn(s) Cu2(aq) ? Sn2(aq) Cu(s)
20
???????????? 9.3 ??? 1 (?)
?????????????????????????????????
????????????????????????????????????? ?????????
?????????????????????????
Mg(s)Mg2 (aq) Fe3(aq),Fe2 (aq) Pt (s)
????????????
Mg(s) ? Mg2 (aq) 2e-
????????????
Fe3(aq) e- ? Fe2 (aq)
?????????????????
Mg(s) 2Fe3(aq) ? Mg2(aq) 2Fe2 (aq)
21
???????????? 9.3 ??? 1 (?)
?????????????????????????????????
????????????????????????????????????? ?????????
?????????????????????????
Zn(s)Zn2 (aq,1mol/dm3) H(aq,1 mol/dm3),H2
(g,1atm)Pt (s)
????????????
Zn(s) ? Zn2 (aq) 2e-
????????????
2H(aq) 2e- ? H2 (g)
?????????????????
Zn(s) 2H(aq) ? Zn2(aq) H2 (g)
22
???????????? 9.3 ??? 1 (?)
?????????????????????????????????
????????????????????????????????????? ?????????
?????????????????????????
Fe(s)Fe2 (aq) Cl- (aq),Cl2(g) Pt (s)
????????????
Fe(s) ? Fe2 (aq) 2e-
????????????
Cl2 (aq) 2e- ? 2Cl- (g)
?????????????????
Fe(s) Cl2 (g) ? Fe2(aq) 2Cl- (aq)
23
???????????? 9.3 ??? 1 (?)
?????????????????????????????????
????????????????????????????????????? ?????????
?????????????????????????
Pt(s)Sn2 (aq),Sn4(aq) Cr (aq),Cr2 (aq)
Pt (s)
????????????
Sn2 (aq) ? Sn4 (aq) 2e-
????????????
Cr2 (aq) e- ? Cr (g)
?????????????????
Sn2 (aq) 2Cr2 (aq) ? Sn4(aq) 2Cr (aq)
24
???????????? 9.3 ??? 2 (?)
??????????????????????????????????????????????????
???????
Zn(s) Pb2(aq) ? Zn2(aq) Pb(s)
Zn(s)Zn2 (aq) Pb2(aq)Pb(s)
???????????? 9.3 ??? 2 (?)
??????????????????????????????????????????????????
???????
Fe(s) Sn4(aq) ? Fe2(aq) Sn2 (aq)
Fe(s)Fe2 (aq) Sn2(aq),Sn4(aq) Pb(s)
25
???????????? 9.3 ??? 2 (?)
??????????????????????????????????????????????????
???????
H2 (g) 2Ag(aq) ? 2H(aq) 2Ag(s)
Pt(s)H2(g) H (aq) Ag(g)Ag(s)
???????????? 9.3 ??? 2 (?)
??????????????????????????????????????????????????
???????
2Cr(s) 3Fe2(aq) ? 2Cr3(aq) 3Fe (s)
Cr(s)Cr3 (aq) Fe2(aq) Fe(s)
26
???????????? 9.3 ??? 3
??????????????????????????????? AgNO3 0.1 mol/dm3
??????????????????????????????????????????????????
??????????????????????????????
?. ???????????????????????????????????????????
?. ?????????????????????????? ????????????????????
?????????
Cu(s) ?
2e-
Cu2 (aq)
Ag(aq) ?
e-
2
2
Ag (s)
2
??????????????????????????????
Cu (s) 2Ag(aq) ? Cu2(aq) Ag (s)
27
???????????? 9.3 ??? 3
??????????????????????????????? AgNO3 0.1 mol/dm3
??????????????????????????????????????????????????
??????????????????????????????
?. ???????????????????????????????????????????
?. ?????????????????????????? ????????????????????
?????????
????????????
Cu(s) ?
2e-
Cu2 (aq)
????????????
? Ag (s)
Ag(aq)
e-
???????????
Cu(s)Cu2 (aq) Ag(aq)Ag(s)
28
I
I
e-
e-
???? ??
???? ???
???? anode
????cathode
Cu2(aq) 2e- ? Cu(s)
Zn(s) ? Zn2(aq) 2e-
Zn(s) / Zn2(aq) // Cu2(aq) / Cu(s)
?????????? ???????????????????????????????
????????????????????????????
?????????????????????? (Electrode potential , E )
Ecathode gt Eanode
Ecell Ecathode Eanode
29
- ?????????????????????????????????????????
- cell voltage
- electromotive force (emf)
- cell potential
Zn (s) Zn2 (1 M) Cu2 (1 M) Cu (s)
Ecathode Eanode Ecell
E Cu/Cu2 E Zn/Zn2 1.10 V
??????????????????????
E(V)
Cu2(s) 2e- ? Cu(s)
???????
Zn2(s) 2e- ? Zn(s)
???????
30
????????????????? (Standard reduction potential
E0 )
??????????????????????????????????????????????????
???????????? ??? ????????????????????? 1 M
?????????????????? 1 atm
Standard Hydrogen Electrode (SHE)
2H (1M) 2e- ? H2(g,1 atm) E0 0.00 V
31
Zn2 (1M) 2e- ? Zn(s) E0 -0.76 V
Zn (s) Zn2 (1 M) H (1 M) H2 (1 atm) Pt
(s)
32
Cu2 (1M) 2e- ? Cu(s) E0 0.34 V
Pt (s) H2 (1 atm) H (1 M) Cu2 (1 M) Cu
(s)
33
?????????????????
- E0 ????????????????????????????????
- ??? E0 ???????????????????????????????????????????
?????????? - ????????????????????????????????
- ???????????????????????
????????????????????????? E0 - ???????????????????????????????????????????? ???
E0 ??????????
34
?????????????????????????(E0)?????????????
1. ???????????????????????????????????????????
????????????????
??? E0
????????????
Ag(aq) e- ? Ag(s) E0
0.80 V
Cu2(aq) 2e- ? Cu(s) E0
0.34 V
2H(aq) 2e- ? H2 (g) E0
0.00 V
Zn2(aq) 2e- ? Zn(s) E0
-0.76 V
??????????
35
?????????????????????????(E0)?????????????
2. ??????????????????????????????????????
(E0cell)
???????????? Ag(s)/Ag(aq,1M) ????????????????
Zn(s)/Zn2(aq, 1 M)
????????
????????????????????????????????????????????
??????
?????????????????????????????? Ag(s)/Ag(aq)
??????? Zn(s)/Zn 2(aq)
?????????? Ag(s)/Ag(aq) ??????????????????????
Ag ????????????? ?????????
E0cell E0cathode E0anode
E0cell E Ag/Ag - E Zn/Zn 2
0.80 V - (-0.76 V)
1.56 V
??? E0cell 1.56 V
36
?????????????????????????(E0)?????????????
3. ??????????????????????????????????????????????
??????????????
??????????????????????????????????
??????????? 1
?????????????Zn ???????????????HCl
??????????????? H2
??????????????????? Zn (s) ? Zn2(aq) 2e-
Zn ?????????????
??????
????????????????? 2H (aq) 2e-? H2 (g)
H 2 ?????????????
E0cell E0cathode E0anode
E0cell E H2 /H - E Zn/Zn 2
0.00 V - (-0.76
V)
0.76 V
??? E0cell ???????????? ????????????????????????
??????????????
37
?????????????????????????(E0)?????????????
3. ??????????????????????????????????????????????
??????????????
??????????????????????????????????
??????????? 2
????????????? Cu ???????????????HCl
??????????????? H2 ???????
?????????????????????? Cu (s) ? Cu2(aq) 2e-
Cu ?????????????
??????
????????????????? 2H (aq) 2e-? H2 (g)
H 2 ?????????????
E0cell E0cathode E0anode
E0cell E H2 /H - E Cu/Cu 2
0.00 V - (0.34
V)
-0.34 V
??? E0cell ??????????? ?????????????????????????
?????????????
????????????????????Cu ????????????? HCl
????????????? H2
??????????????????????? ?????????????????????????
?????????????
38
????????????????? E0
- ?????????????????????????????????????
- ??????????????????????
? E0 ?????????? ??????????????????
- ????????????????????????? ???????
- ??????????????????
? E0 ????????? ???????????????????
????????????????????????
- ???????????????????????? ??????????
- ?????????????
39
???????????????????????, Ecell
Ecell Ecathode - Eanode
???????????????
E0cell E0cathode - E0anode
?????????????? Ecell
??????? ???????????????????
?????? ??????????????????????
40
??????????????? (Nernst Equation)
?????????
Ecell ?????????????????????? E0cell
????????????????????????????? R
???????????????, 8.314 J K-1 mol-1 T
??????????????????? (K) n ????? e-
?????????????????????? F ???????????
Faraday ? 96500 C
41
(No Transcript)
42
- Ecell ??????????????????????
- E0cell ?????????????????????????????
- R ???????????????, 8.314 J K-1 mol-1
- T ??????????????????? (K)
- n ????? e- ??????????????????????
- F ??????????? Faraday ? 96500 C
- (2.303RT)/F 0.059
43
?????????????
44
???????? ?????????????????????? Cd/Cd2(0.015
M) ???????? E0Cd -0.403 V
E -0.457 V
45
???????? ??????????????????????? 25? c
????????????
???
k 2 x 1037
46
???????????????? (Concentration cell)
????????????????????????????????? ? anode
????????????????????????????????? ? cathode
47
???????????????? (Concentration cell)
48
Cu/CuSO4 (0.1M) // CuSO4 (1.0 M)/Cu
Anode
Cathode
49
????
50
?????????????
- ???????????????????????
- (primary galvanic cell)
- ?????????????????????????
- (secondary galvanic cell)
- ???????????????????
- ???????????????????
51
?????????
Anode
Cathode
52
- ????????????????????????????????? Zn2
????????????????
53
?????????
Mercury Battery
Anode
Cathode
54
??????????????????????-????????
fuel cell ?????????????????? ?????????????????????
? ????????????????????????????????????????????????
Anode
Cathode
55
???????????????????????
Lead storage battery
Anode
Cathode
56
??????????????????????? ???
??????????? 9.4 ???9.5 ????????