Apresenta - PowerPoint PPT Presentation
1 / 53
Title:
Apresenta
Description:
Title: Apresenta o do PowerPoint Author: Usuario Last modified by: Windows Created Date: 5/19/2003 5:42:26 PM Document presentation format: Personalizar – PowerPoint PPT presentation
Number of Views:51
Avg rating:3.0/5.0
Title: Apresenta
1
(No Transcript)
2
Transporte de élétrons e fosforilação
oxidativa 1 - Introdução 2 - Formas de
formação de ATP 3 - Mitocondria
características gerais componentes da cadeia 4
- Óxido redução conceitos, organização dos
componentes da cadeia de acordo com
seus potenciais de óxido redução 5 - Esquema
geral de funcionamento da cadeia de transporte de
e- 6 - Inibidores e desacopladores do Sistema 7
- Produção de ATP por molécula de glicose
Aproveitamento de NADH citoplasmático através
de lançadeiras 8 - Produção de calor 9 -
Regulação do Sistema
3
Metabolismo integração entre catabolismo e
anabolismo
4
Estágio 1 Produção de Acetil-CoA
Catabolismo de proteínas lipídeos e
carboidratos
mitocôndrias
Estágio 2 Oxidação de Acetil-CoA
Estágio 3 Transporte de elétrons
e fosforilação oxidativa
5
Localização da glicólise e do ciclo de Krebs
(tricarboxilicos ou dos ácidos cítricos) e do
transporte de elétrons e fosforilação
Citoplasma
Interior da mitocôndria
6
Transporte de élétrons e fosforilação
oxidativa 1 - Introdução 2 - Formas de
formação de ATP 3 - Mitocondria
características gerais componentes da cadeia 4
- Óxido redução conceitos, organização dos
componentes da cadeia de acordo com
seus potenciais de óxido redução 5 - Esquema
geral de funcionamento da cadeia de transporte de
e- 6 - Inibidores e desacopladores do Sistema 7
- Produção de ATP por molécula de glicose
Aproveitamento de NADH citoplasmático através
de lançadeiras 8 - Produção de calor 9 -
Regulação do Sistema
7
Os produtos formados na hidrólise do ATP são mais
estáveis porque fazem ressonância e apresentam
menos repulsão eletrostática
8
Existem duas formas de formação do ATP
(nos animais)
1 Fosforilação ao nível de Substrato 2
Fosforilação através da cadeia transportadora
de elétrons acoplada a fosforilação
9
Gliceraldeido 3-fosfato desidrogenase
(1)
Produto desta reação contém energia para
fosforilar ADP em ATP
- Enzima da via glicolítica
- NADH produzido no citoplasma
- Destino do NADH em meio aeróbico e meio
anaeróbico
10
Fosforização ao nível de substrato
(1)
- Conversão do succinil-CoA em succinato
- Etapa de fosforilação da enzima
- GTP ou ATP (?Gº 0)
11
Mecanismo da reação da succinil-CoA sintetase
Inicialmente o succinil-CoA se liga à enzima
succinil-CoA sintetase.
No passo 1, um grupo fosforil ocupa o lugar da
CoA no succinil-CoA ligado a enzima, formando um
composto acila-fosfato de alta energia. No passo
2, o succinil-fosfato cede seu grupo fosforil
para um resíduo de histidina da cadeia
polipeptídica da enzima, formando um derivado de
alta energia. No passo 3, o grupo fosforil é
transferido desse resíduo de His para o grupo
fosfato terminal da molécula de GDP (ADP)
formando GTP (ATP).
12
Transporte de élétrons e fosforilação
oxidativa 1 - Introdução 2 - Formas de
formação de ATP 3 - Mitocondria
características gerais componentes da cadeia 4
- Esquema geral de funcionamento da cadeia de
transporte de e- 5 - Óxido redução conceitos,
organização dos componentes da cadeia
de acordo com seus potenciais de óxido redução 6
- Inibidores e desacopladores do Sistema 7 -
Produção de ATP por molécula de glicose
Aproveitamento de NADH citoplasmático através de
lançadeiras 8 - Produção de calor 9 - Regulação
do Sistema
13
(No Transcript)
14
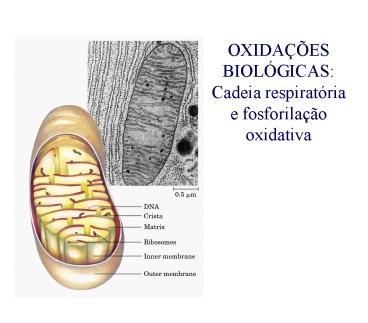
Estrutura da mitocondria
- Membrana externa
- Membrana interna
- Matriz mitocondrial
15
Estudo dos componentes da membrana mitocondrial
16
Complexos proteícos transportadores de elétrons
O que são grupos prostéticos?
17
COMPONENTES DA CADEIA RESPIRATÓRIA
COMPLEXO I recebe elétrons do NADH COMPLEXO II
recebe elétrons do FADH2 UBIQUINONA (Q) COMPLEXO
III CITOCROMO c e COMPLEXO IV
18
FOSFORILAÇÃO OXIDATIVA DO ADP
2H
4H
4H
19
O gradiente eletroquímico de prótons gerado
durante o transporte de elétrons é usado para
síntese de ATP através do complexo ATPsintase
20
Modelo mostrando a síntese de ATP
Proteínas transportadoras de eletrons Proteínas
integrais e periféricas Extrusão de
prótons Complexo ATP sintase Gradiente
químico Gradiente elétrico Gradiente
eletroquímico
21
Transporte de élétrons e fosforilação
oxidativa 1 - Introdução 2 - Formas de
formação de ATP 3 - Mitocondria
características gerais componentes da cadeia 4
- Esquema geral de funcionamento da cadeia de
transporte de e- 5 - Óxido redução conceitos,
organização dos componentes da cadeia
de acordo com seus potenciais de óxido redução 6
- Inibidores e desacopladores do Sistema 7 -
Produção de ATP por molécula de glicose
Aproveitamento de NADH citoplasmático através de
lançadeiras 8 - Produção de calor 9 - Regulação
do Sistema
22
Potencias de óxido-redução
23
Reações de óxido-redução
Ared Aox e-
oxidação As formas oxidada e reduzida
do composto (Ared / Aox ) constituem um sistema
chamado par redox. Box e-
Bred redução Ared
Box Aox Bred
reação de óxido-redução Nas reações
de óxido redução biológicas, os elétrons
transferidos são geralmente acompanhados de
prótons ou seja há transferência de átomos de
hidrogênio AH2 B
A BH2 (red) (ox)
(ox) ( red) A tendência do par
redox (Ared / Aox ) em perder ou ganhar
elétrons é expressa pelo seu potencial de
óxido-redução, representado por E que depende das
espécies envolvidas e das concentrações da forma
oxidada e reduzidas das espécies.
24
(No Transcript)
25
- Uma vez conectadas as meias células, os elétrons
fluem de uma meia célula para outra - Se a reação se proceder na seguinte direção
- X- H X ½ H2
- Nas meias células as reações serão
- X- X e-
- H e- ½ H2
- Os eletrons fluem da meia célula onde está a
substância teste (X) para a meia célula de
referência ( padrão) - Dessa forma , o eletrodo é negativo em relação ao
eletrodo padrão. - O potencial redox do par H H2 é definido como
sendo 0 V (volts) - Potencial negativo significa que um substrato tem
menor afinidade por elétrons do que H2 - Potencial positivo significa que um substrato tem
maior afinidade por elétrons que H2
26
OXIDAÇÃO DO NADH ATÉ OXIGÊNIO
Potenciais de óxido-redução
NAD H 2e-
NADH Eo' - 0,32V ½O2 H 2e-
H2O Eo' 0,82V
A reação acontecerá da seguinte
forma ½O2 NADH H
H2O NAD ?Eo' 1,14 V
?Eo' Eo' do oxidante - Eo' do redutor
0,82 - ( - 0,32) 1,14 V
?Go' - nF.?Eo' -2 x 96.500 x
0,82 - (- 0,32) - 220 kJ /mol
Aplicando a equação
27
- Um forte agente redutor, como NADH e FADH2 tem
potencial redox negativo - Um forte agente oxidante, como O2 , tem
potencial redox positivo - A variação de energia livre de uma reação de
oxido-redução pode ser facilmente calculada
somente avaliando a diferença de potencial redox
dos reagentes e produtos.
28
(No Transcript)
29
Proteínas transportadoras de eletrons
Complexo I NADH desidrogenase Complexo II
succinato desidrogenase Complexo III ubiquinona
citocromo c oxidoredutase Citocromo c Complexo
IV citocromo oxidase
30
NADH ubiquinona oxidoredutase
NADH desidrogenase (FMN) 2H 2e-
NADH desidrogenase (FMNH2) flavina
mononucleotídeo é derivado da riboflavina
(vitamina B2) Os centros Fe-S não recebem protons
, são transportadores de eletrons. Fe3 para
Fe2. Os protons são transferidos para o espaço
intermembrana. Primeira etapa na formação do
gradiente de prótons.
31
Complexo II também chamado de succinato
desidrogenase. A enzima succinato desidrogenase
faz parte do complexo
Grupo prostéticos FAD e centros Fe-S Eletrons
são transferidos do succinato ao FAD, aos centros
Fe-S e depois para a ubiquinona (Q).
Outras desidrogenases acil-CoA desidrogenase da
ß-oxidação transfere os eletrons para a enzima
transferidora de eletrons (ETF) que tem o FAD
como grupo prostético e depois para a ETF
ubiquinona oxidoredutase e finalmente para a
ubiquinona.
32
Aproveitamento do NADH do citosol gerado na
glicólise
33
Coenzima Q ou ubiquinona
Cadeia lateral composta de unidades isoprênicas.
Não é uma proteína. Naureza hidrofóbica
mobilidade na fase lipídica da membrana. Recebe
2 protons e dois eletrons e se torna reduzida
(ubiquinol).
34
O ion Ferro presente no grupo heme é o
responsável pela capacidade de transferência de
eletrons destas proteínas, alternado seu estado
de oxidação de Fe2 e Fe3. O grupo heme varia de
citocromo para citocromo conforme seus grupos
substituintes. Também diferem quanto aos ligantes
axiais do ion ferro.
35
Complexo citocromo bc1 ou ubiquinona citocromo c
oxido redutase (complexo III)
Constituído de dois citocromos b (b562 e b566),
por um centro Fe-S e pelo citocromo C1. Os
eletrons da coenzima Q são transferidos para o
complexo III e os prótons são transferidos para
para o espaço intermembrana.
Sítios de ação de drogas que inibem a
fosforilação oxidativa antimicina e mixotiazol.
36
Complexo IV transfere eletrons para o oxigênio.
Também é chamado de citocromo c oxidase.
Apresenta dois citocromos do tipo a (a e a3) e
dois íons cobre, cada qual associado a um dos
dois citocromos. Estados de oxidação do cobre
Cu2 e Cu1. O complexo IV é responsável pela
doação de quatro eletrons para a molécula de
oxigênio, que ligando-se aos prótons do meio
converte-se em H2O. 95 de todo oxigênio
consumido é utilizado nesta operação e são
produzidos cerca de 300 ml de água, chamada de
água metabólica (humanos). Animais que hibernam e
animais que passam longos períodos sem ingerir
água (camelos) utilizam a água metabólica.
37
(No Transcript)
38
O ?G (força próton-motora) resultante do
gradiente químico e do gradiente elétrico, é
capaz de realizar a síntese de ATP.
39
A PRODUÇÃO DE ATP É ENZIMÁTICA
40
Complexo ATP sintase compreende dois
componentes cada componente é constituído de
várias cadeias polipeptídicas. Uma porção,
esférica, chamada de fator de acoplamento 1 (F1)
que contém os sítios de síntese de ATP. A segunda
porção fica embebida na membrana interna
mitocondrial interna, constituindo um canal para
a entrada de prótons (Fo ) assim chamado porque
contém um sítio de ligação para a oligomicina, um
inibidor da ATP sintase.
41
COMPONENTES DA FoF1ATPase
42
Transporte de élétrons e fosforilação
oxidativa 1 - Introdução 2 - Formas de
formação de ATP 3 - Mitocondria
características gerais componentes da cadeia 4
- Óxido redução conceitos, organização dos
componentes da cadeia de acordo com
seus potenciais de óxido redução 5 - Esquema
geral de funcionamento da cadeia de transporte de
e- 6 - Inibidores e desacopladores do Sistema 7
- Produção de ATP por molécula de glicose
Aproveitamento de NADH citoplasmático através
de lançadeiras 8 - Produção de calor 9 -
Regulação do Sistema
43
(No Transcript)
44
ADP e Pi são substratos para a ATP
sintase. Succinato é o substrato da Succinato
Desidrogenase Cianeto é uma droga que inibe a
citocromo c oxidase (inibe o transporte de
elétrons)
Venturicidina e oligomicina inibem o complexo Fo
(inibem a ATP sintase). DNP é um carreador de
prótons hidrofóbicos (desacoplam a Fosforilação
do transporte de elétrons).
45
Desacopladores são compostos que dissociam o
transporte de elétrons da síntese de
ATP. Exemplo DNP e FCCP dissipam o gradiente
de prótons.
46
Adenina nucleotídeo translocase e fosfato
translocase
A produção de ATP acontece interligada a
processos de transporte
ATP/ADP ?
ATP/ADP ?
47
Transporte de élétrons e fosforilação
oxidativa 1 - Introdução 2 - Formas de
formação de ATP 3 - Mitocondria
características gerais componentes da cadeia 4
- Óxido redução conceitos, organização dos
componentes da cadeia de acordo com
seus potenciais de óxido redução 5 - Esquema
geral de funcionamento da cadeia de transporte de
e- 6 - Inibidores e desacopladores do Sistema 7
- Produção de ATP por molécula de glicose
Aproveitamento de NADH citoplasmático através
de lançadeiras 8 - Produção de calor 9 -
Regulação do Sistema
48
NADH via lançadeira glicerol fosfato 1,5
ATP NADH via lançadeira malato-aspartato 2,5
ATP
NADH 2,5 ATP FADH2 1,5 ATP
49
Aproveitamento do NADH do citosol gerado na
glicólise
50
Lançadeira malato-aspartato
51
Transporte de élétrons e fosforilação
oxidativa 1 - Introdução 2 - Formas de
formação de ATP 3 - Mitocondria
características gerais componentes da cadeia 4
- Óxido redução conceitos, organização dos
componentes da cadeia de acordo com
seus potenciais de óxido redução 5 - Esquema
geral de funcionamento da cadeia de transporte de
e- 6 - Inibidores e desacopladores do Sistema 7
- Produção de ATP por molécula de glicose
Aproveitamento de NADH citoplasmático através
de lançadeiras 8 - Produção de calor 9 -
Regulação do Sistema
52
- FORMAÇÃO DE CALOR
- (tecido adiposo marron)
- Esta proteína que tem a sigla
- em inglês de UCP, é a
- principal produtora de calor
- em mamíferos.
- Ocorre principalmente
- em animais que hibernam.
- Também tem relação com
- diferenças no metabolismo
- entre as diferentes pessoas.
- A energia derivada do
- transporte de elétrons é
- liberada como calor.
UCP
53
Regulação do Sistema
- Transporte de elétrons e a síntese de ATP são
processos intimamente relacionados. - Os substratos deste processo são coenzimas
reduzidas, oxigênio, ADP e Pi. - O limitante destes processos é a concentração
- de ADP. Daí é o regulador mais importante.
- A regulação da velocidade de oxidação das
coenzimas exercida pela concentração
de - ADP chama-se controle respiratório.
- As vias que dependem da reciclagem das
coenzimas oxidadas pela cadeia de transporte - de elétrons (por exemplo, o ciclo de Krebs)
dependem da razão ATP/ADP. O próprio ADP
participa das regulações das enzimas alostéricas.