Les insulines - PowerPoint PPT Presentation
1 / 27
Title:
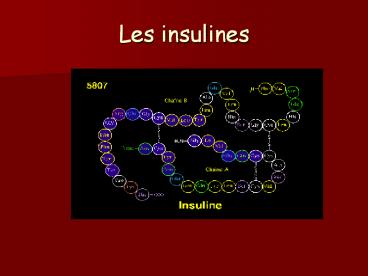
Les insulines
Description:
Title: Les insulines Author: Corinne Last modified by: Corinne Created Date: 8/15/2006 3:25:27 PM Document presentation format: Affichage l' cran – PowerPoint PPT presentation
Number of Views:126
Avg rating:3.0/5.0
Title: Les insulines
1
Les insulines
2
Insulinothérapie histoire
- Début 1900 Drs Banting, Best et Mac Leod
isolent une substance hypoglycémiante du pancréas
de chien qui agit sur les chiens diabétiques
après ablation de pancréas - James Collip, chimiste arrive à purifier
cette substance extraite de pancréas de bœuf - 11 janvier 1922 1ère injection à Léonard
Thomson, 14 ans - Avril 1922 nom de la substanceinsuline (latin
insula) - 1923 Compagnie Lilly (USA) et laboratoire
Connaught (Toronto) se lancent dans la production
industrielle - 1926 cristallisation de linsuline par JJ Abel
- 1934 Hagedorn (pharmacologue danois) fabrique la
1ère insuline au zinc et en 1946 la NPH qui porte
son nom - 1951 Novo commercialise des insulines au zinc
amorphes, cristallines, de très longue durée
daction (12-18h)
3
Insulinothérapie histoire
- 1958 Frédéric Sanger découvre la séquence
dacides aminés de linsuline de boeuf (prix
Nobel) - Fin des années 1970 insulines monocomposées
(Novo) utilisation de linsuline de porc, de
structure plus proche de celle de lhomme - Hémisynthèse de linsuline humaine à partir de
celle du porc (1 acide aminé diffère) - 1979 fabrication par génie génétique (Lilly)
avec E. coli - 1986 génie génétique avec Saccharomyces (Novo)
- Fin des années 1990 analogues de linsuline
rapidité daction - 2006 insuline inhalée
4
Insulinothérapie histoire
5
Insulinothérapie histoire
6
Les nouvelles insulines
- Analogue lent insuline détémir LEVEMIR
(NovoNordisk) stylos (flexpen) 3 ml, cartouches
3 ml délai daction 1 heure Cmax 6-8
heures durée daction 12 à 24 heures - Analogue rapide insuline glulisine APIDRA
(Sanofi-Aventis) flacons 10 ml, stylos 3 ml
(optiset), cartouches 3 ml - Insuline humaine par voie inhalée EXUBERA
(Pfizer) 1 (3 UI) ou 3 mg (8 UI) dinsuline
humaine
7
Les insulines humaines rapides
- Début daction environ 15 minutes
- Agissent 4 à 6 heures
- Limpides
- Durée daction dose dépendante
Début Pic Durée
ACTRAPID Novo Nordisk 30 min 1-3 h 8 h
UMULINE RAPIDE Lilly 30 min 1-3 h 5-7 h
INSUMAN RAPIDE Aventis 30 min 1-4 h 7-9 h
8
Les analogues rapides
- Début daction quelques minutes
- Durée daction 2 à 6 heures, peu dose dépendante
- Limpides
- Meilleur contrôle des glycémies postprandiales
- Moins dhypoglycémies à distance des repas
Début Pic Action
APIDRA Aventis 10-20 min 1 h 4-6 h
HUMALOG Lilly 15 min 30min à 1 h 2-5 h
NOVORAPID Novo Nordisk 10-20 min 1-3 h 3-5 h
9
Les insulines intermédiaires
- Délai daction 30 à 45 min
- Durée daction 10 à 16 heures
- Action plus importante au cours des 6 premières
heures - Aspect laiteux, homogénéiser avant injection
- Protamine fixation dune quantité précise
dinsuline (saturation des sites de fixation)
mélanges avec insulines rapides - Insulines zinc plus commercialisées
10
Les insulines humaines intermédiaires
Début Pic Durée
Les insulines humaines intermédiaires NPH Les insulines humaines intermédiaires NPH Les insulines humaines intermédiaires NPH Les insulines humaines intermédiaires NPH Les insulines humaines intermédiaires NPH
INSULATARD NPH Novo Nordisk 1h30 min 4-12 h Jusquà 24 h
INSUMAN BASAL Aventis 1 h 3-4 h 11-20 h
UMULINE NPH Lilly 1 h 2-8 h 18-20 h
11
Les analogues lents
- Début daction 1 à 2 heures
- Durée daction 12 à 24 heures
- Limpides
Délai Pic Durée
LANTUS Aventis 1 h - 24 h
LEVEMIR Novo Nordisk 1 h - 12-24 h
12
Les mélanges dinsulines
- Prêt à lemploi ou non
- Insuline NPH insuline ou analogue rapide
(LANTUSAPIDRA?) - Durée daction 12 heures environ
- Chiffre indiqué insuline rapide
- Intérêt du mélange fait soi-même adapter
séparément les doses dinsuline rapide et
intermédiaire
13
Les mélanges dinsulines
Début Pic Durée
Les mélanges fixes dinsuline humaine Les mélanges fixes dinsuline humaine Les mélanges fixes dinsuline humaine Les mélanges fixes dinsuline humaine Les mélanges fixes dinsuline humaine
MIXTARD Novo Nordisk 30 min 2-8 h Jusquà 24 h
UMULINE PROFIL 30 Lilly 30 min 1-8 h 18-20 h
INSUMAN COMB 15, 25 Aventis 30 min à 1 h 2-4 h 12-19 h
INSUMAN COMB 50 Aventis 30 min 1h30 à 4 h 12-16 h
Les analogues mélanges fixes Les analogues mélanges fixes Les analogues mélanges fixes Les analogues mélanges fixes Les analogues mélanges fixes
NOVOMIX 30 Novo Nordisk 10-20 min 1-4 h Jusquà 24 h
HUMALOG MIX 25 Lilly 15 min 30-70 min 15 h
HUMALOG MIX 50 Lilly 15 min 30-70 min 15 h
14
Les sites dinjection
15
Linsuline détémir LEVEMIR
16
Linsuline détémir LEVEMIR
- Novo Nordisk
- 2ème analogue lent mis sur le marché
- Biotechnologie à partir de Saccharomyces
cerevisiae - Différences avec insuline humaine thréonine en
position 30, acide myristique (acide gras saturé
dorigine végétale) en position B29 - Phénol (conservateur) excipient à effet notoire
- pH 7,4
- Solution limpide, ne nécessite pas de remise en
suspension avant injection - Présentations stylos (Flexpen), cartouches
(Penfill)
17
Linsuline détémir LEVEMIR
- Acide myristique se lie à lalbumine dans les 3
compartiments (tissu SC, sang, tissu cible) 3
espaces de prolongement de durée daction - Meilleure affinité pour les récepteurs à
linsuline que pour lalbumine
18
Linsuline détémir LEVEMIR
- Essais cliniques Type I versus NPH, en ouvert
- 9 études et une méta-analyse 3188 patients
- Durée 4 à 6 mois
- HbA1c (critère principal) non infériorité dans 6
essais, non significatif 1 essai, significatif 2
essais ( p ?) - Glycémies à jeun plus basses que pour la NPH
(critère secondaire) - Moins de variabilité intra-individuelle dans les
glycémies à jeun (critère secondaire) - Pourcentage de patients à 2 injections/jour?
19
Linsuline détémir LEVEMIR
- Essais cliniques Type II versus NPH en ouvert
- 4 études, 1841 patients
- Durée 4 à 6 mois
- Metformine (étude 1337) ou traitement habituel
sauf glitazone - HbA1c (critère principal) non infériorité dans 1
essai, non significatif 2 essais, significatif 1
essai ( p ?) - Glycémies à jeun plus basses que pour la NPH dans
2 études (critère secondaire) - Moins de variabilité intra-individuelle dans les
glycémies à jeun dans 3 études sur 4 (critère
secondaire) - Pourcentage de patients à 2 injections/jour?
20
Linsuline détémir LEVEMIR
- ? hypoglycémies pas dans toutes les études
- Réactions au point dinjection importantes (1,3
versus 0,2 sous NPH type I et 2,4 versus 1,7
sous NPH type II) - 11 décès sur 13 ont concerné des patients sous
LEVEMIR - Moindre prise de poids sous LEVEMIR dans toutes
les études - Ac anti insuline EMEA demande de données à
long terme
21
Linsuline glulisine APIDRA
22
Linsuline glulisine APIDRA
- Sanofi Aventis
- 3ème analogue rapide mis sur le marché
- Biotechnologie à partir dE. coli
- Différences avec insuline humaine lysine en B3
au lieu de asparagine et acide glutamique en B29
au lieu de lysine - Metacresol (conservateur)
- pH 7,3
- Solution limpide, ne nécessite pas de remise en
suspension avant injection - Présentations stylos (Optiset), flacons
23
Linsuline glulisine APIDRA
- Essais cliniques 3 type I, 1 type II
- Randomisées, en ouvert, non infériorité
- Comparateurs
- Type I lispro, aspart, insuline rapide humaine
- Type II insuline rapide humaine
- Durée 3 à 8 semaines
- Type I pas de différence en terme dHbA1c
- Type II
- différence significative sur lHbA1c en faveur de
la glulisine (0,16 impact clinique?) - moins de variabilité des glycémies post
prandiales - Tolérance celle des autres analogues taux
dhypoglycémies comparables entre les 2 groupes
24
Linsuline glulisine APIDRA
- Variations de lHbA1c (critère principal) à 26
semaines
- ASMR V type I
- ASMR IV type II
25
Linsuline inhalée EXUBERA
26
Linsuline inhalée EXUBERA
- Laboratoire Pfizer
- Approuvée par la FDA pour le traitement du
diabète de type I et II de ladulte - Ampoules de 1 ou 3 mg dinsuline sous forme de
poudre sèche soit approximativement 3 ou 8 UI
dinsuline ordinaire injectable SC - Inhalateur introduction des ampoules pression
sur la poignée du dispositif libération dun
nuage dinsuline inhalation absorption vers les
capillaires pulmonaires. - Début deffet 32 min
- Durée daction 387 min (plus que lispro, moins
que linsuline ordinaire) - Essais pas de différence en terme dHbA1c chez
les type I (versus NPH insuline ordinaire) et
le type II (versus différents ADO)
27
Linsuline inhalée EXUBERA
- Augmentation des hypoglycémies sévères
- Taux élevés danticorps anti-insuline
- Toux légère à modérée juste après linhalation,
tend à diminuer avec le temps - Altération des fonctions pulmonaires
- Examen des fonctions pulmonaires en début de
traitement, après 6 mois puis annuellement - Interrompre le traitement si le VEMS (Volume
Expiratoire Maximal par Seconde) diminue de plus
de 20 par rapport à la valeur initiale - Satisfaction bonne les patients ayant le
choix préfèrent en majorité (gt 80) linsuline la
voie inhalée par rapport à la SC - Dispositif dadministration encombrant
- Sensibilité à lhumidité risque de sous dosage
- Nécessité de plusieurs prises journalières